Hovedforskjell: Atomer er de grunnleggende enhetene som alle saken er laget av. Atomer er små, fra 0, 1 til 0, 5 nanometer i bredde. Hvert atom av ethvert element består av protoner, nøytroner og elektroner. Atomer av forskjellige elementer kommer sammen for å lage molekyler. Dette skjer via en kjemisk reaksjon. Et molekyl er den minste mengden av et kjemisk stoff som kan eksistere.
Et element er et rent kjemisk stoff som har en eller en type atom, preget av atomnummeret. Atomenummeret er avledet fra antall protoner som er tilstede i elementets kjernen. Det er totalt 118 elementer som er identifisert, fordelt mellom metall, metalloider og ikke-metaller. Hvert element har sitt eget sett med egenskaper. De fleste elementene er tilgjengelige på jorden, mens noen få har blitt utviklet kunstig gjennom atomreaksjoner. Et element er allerede i rawest form og kan ikke brytes ned lenger. Alle elementene finnes i periodisk tabell, oppført med atomnummer.
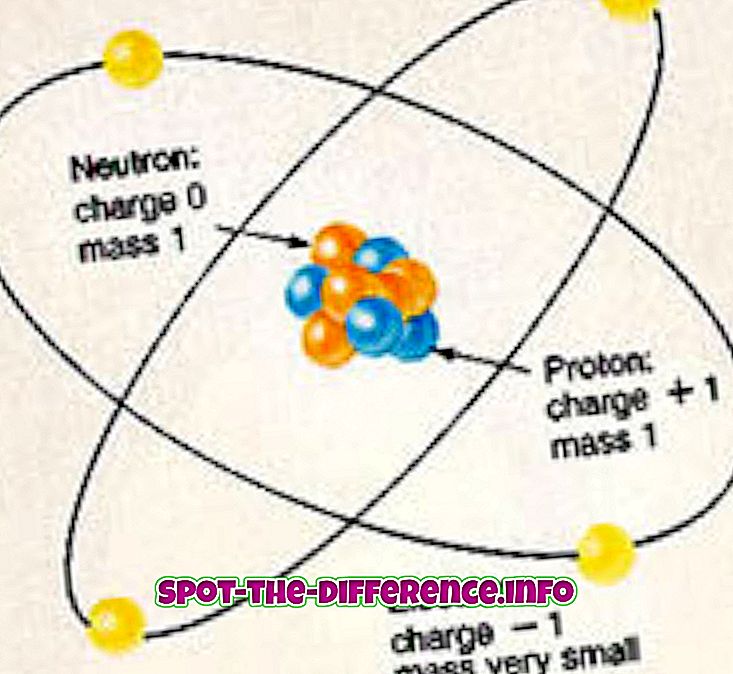
Hvert atom av ethvert element består av protoner, nøytroner og elektroner. Protonene og nøytronene utgjør atomkernen og ligger i midten av atomet. Kjernen er omgitt av en sky av elektroner som er bundet til kjernen av en elektromagnetisk kraft. Elektronene har en negativ ladning som er hvordan de tiltrekkes til kjernen, da protonene i kjernen har en positiv ladning. Neutroner, derimot, har ingen kostnad.
Antallet protoner, nøytroner og elektroner i et atom bestemmer hvilket element det er. For eksempel: Et atom av jern har 26 protoner, 30 nøytroner og 26 elektroner. Hvert jernatom vil ha denne konfigurasjonen.
Atomer av forskjellige elementer kommer sammen for å lage molekyler. Dette skjer via en kjemisk reaksjon. For eksempel: to hydrogenatomer og ett oksygenatom kombinere for å lage et vannmolekyl.

Et molekyl kan ha svært forskjellige egenskaper fra elementene som den er laget av. For eksempel: Vann oppfører seg veldig annerledes enn enten oksygen eller hydrogen, selv om det består av to hydrogenatomer og ett oksygenatom.
Videre kan et atom ikke eksistere uavhengig i naturen uten å binde seg til noe. Vi vil aldri finne bare et enkelt oksygenatom eller et enkelt karbonatom. Det er alltid bundet til noe, som O2 (oksygen) eller CO2 (karbondioksid). Når molekylet er bundet inn i et molekyl, kan det eksistere uavhengig av naturen, og derfor kan vi alltid finne et oksygenmolekyl, et karbondioksid, et vannmolekyl (H2O) osv.
I et molekyl holdes atomer fast i en bestemt form eller form. Dette er hovedsakelig avhengig av antall obligasjoner som atom kan gjøre. Atomer danner molekyler ved å danne kjemiske bindinger med hverandre. Oksygenatomer har alltid to bindinger med andre atomer, karbonatomer har alltid fire bindinger med andre atomer, og nitrogenatomer har alltid tre bindinger med andre atomer. På grunn av dette har en bestemt type molekyl alltid en bestemt form, slik som femkantet, sekskantet, lateralt, bi-lateralt etc.
Molekyler pleier alltid å gruppere sammen, deres dannelse avhengig av deres tilstand. Som i en gassform, har molekylene en tendens til å være bare flyr rundt. I flytende tilstand har molekylene en tendens til å være løst gruppert slik at de fortsatt kan bevege seg. Mens i en fast tilstand er molekylene tett pakket sammen og kan bare vibrere.
Molekyler er vanligvis representert i en molekylformel. For eksempel: O2, H2O, CO2, C6H12O6 (sukker). Molekylformelen er navnet på elementet etterfulgt av antall atomer av det elementet i molekylet.