Hovedforskjell: Arrangementet av atomer i et molekyl bidrar til å bestemme polariteten. Et molekyl er sies å være polært, hvis det har en positiv og en negativ ladning. Et ikke-polart molekyl er et molekyl med mindre ladning.
I kjemi refererer polaritet til separasjonen mellom elektriske ladninger av et molekyl eller dets kjemiske gruppe som har et elektrisk dipol- eller flerpolet øyeblikk. Polare molekyler interagerer gjennom intermolekylære bindinger og hydrogenbindinger. Molekylærpolaritet er avhengig av forskjellen i elektronegativitet mellom atomer i et molekyl. Polaritet, bestemmer også en rekke fysiske egenskaper som overflatespenning, smeltepunkt og kokepunkter og løselighet.
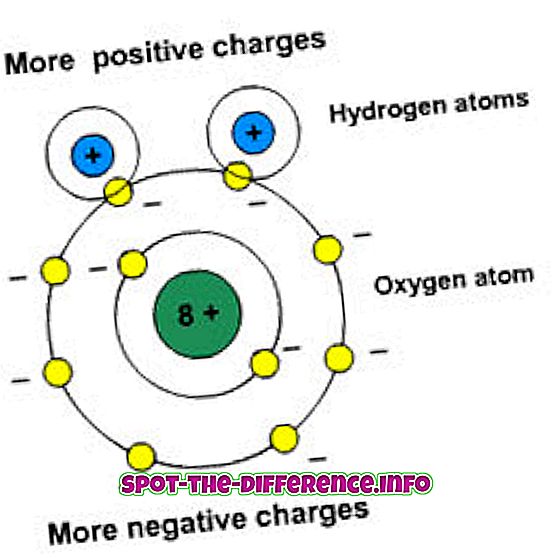
Polaritet betyr separasjon av kostnadene. Disse molekylene har et dipolmoment. Dipole-øyeblikket måler polariteten til et obligasjon. Polare stoffer interagerer med andre polare elementer.

Et ikke-polart molekyl har ikke nok ladning. Ikke-polare molekyler fordeles på en symmetri måte og har ikke mange elektriske ladninger på dem. Når to atomer eller to samme atomer har samme elektronbinding mellom dem, trekker atomene elektronparet. Denne trekk hjelper dem med å dele elektroner, og denne typen bindingsdeling mellom molekyler er kjent som ikke-polare kovalente bindinger.
Sammenligning mellom polar og ikke-polar:
Polar | Non-Polar | |
Definisjon | Polare stoffer har en positiv og en negativ ladning på atomet. | Ikke-polare stoffer har ikke store kostnader på det vedlagte atomen. |
Bevegelse | De har elektrisk dipolbevegelse. | De har ingen dipolbevegelse. |
Charge separasjon | Det er ladestyring. | Det er ingen avgift separasjon. |
Interaksjon | De samhandler med andre polare stoffer. | De interagerer ikke med andre polare stoffer. |
Eksempel | Vann, alkohol og svovel. | Olje. |