Nøkkelforskjell: Atommasse er bare massen av en bestemt isotop, eller den samlede massen av atomets protoner, nøytroner og elektroner. Atometall er antallet protoner som finnes i en kjernen til et element.
La oss innse at kjemien er forvirrende, den forskjellige mengden av elementer, atomnumre, obligasjoner, masse, vekt, atomer, etc. Alle disse ordene begynner å sløre etter en viss tid at en person ikke lenger kan skille den ene fra den andre. God atommasse og atomnummer er to av slike ord som ofte forveksles og brukes om hverandre.
Atommassen er massen av et atom når den er i ro. Dette skyldes at når et atom beveger seg med svært høy hastighet, har det en tendens til å øke i masse. Selv om det ifølge definisjonen er atommassen massen av alle protoner, nøytroner og elektroner, er elektroner for små til å gjøre noen signifikant forskjell i atommassen. De fleste av elementene i periodisk tabell har isotoper og på grunn av forskjellen i nøytrontallet endres også massene av hver isotop.
Atommassen uttrykkes ved hjelp av atommasseenheter eller amu. En atommasse er lik 1/12 av massen av Carbon-12. Når massen av et atom er delt av 1/12 av massen av karbon-12, oppnås den relative massen av elementet. Imidlertid er relativ masse av en gjenstand faktisk atomvekten til et element, som det beregnes ved å betrakte alle isotoper. Selv om dette ikke bør antas som atommasse av et element.

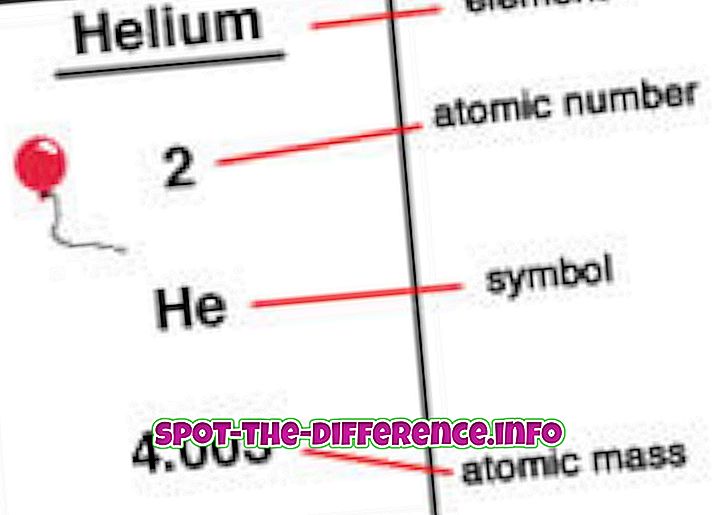
Atometall er antallet protoner som finnes i en kjernen til et element. Når et atom er nøytralt, betyr det at det har samme antall protoner og elektroner. Atomenummer er betegnet med en Z. Siden hvert element har et annet antall protoner, brukes dette tallet også til å representere et element. Isotoper deler vanligvis det samme atomnummeret, men klassifiseres ved hjelp av atommassen, for eksempel Carbon-12, Carbon-13.
Elementer er plassert i rekkefølge av atomnummer på et periodisk bord. Atomenummeret er oppført i det øvre venstre hjørnet av elementet som en oppskrift. Atometall kan bidra til å avsløre informasjon om elementet, og mange kan se atomnummeret og angi hvilket element det er. Det forteller også hvor i det periodiske bordet det kan plasseres og om det er flytende, gass eller fast. Atomnummer gir også informasjon om kjernebelastning, oksidasjonstilstander, bindingsadferd, jonbelastning etc.