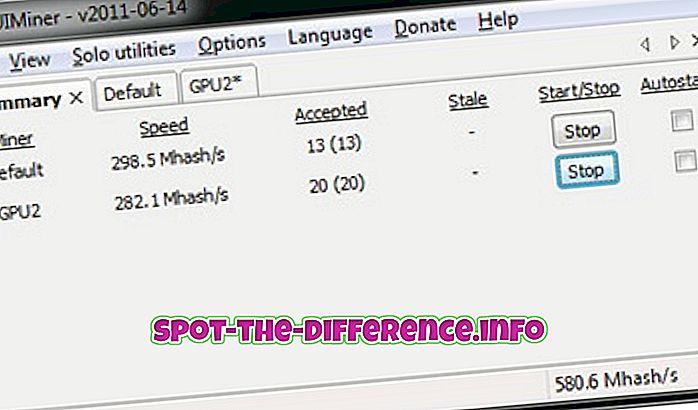
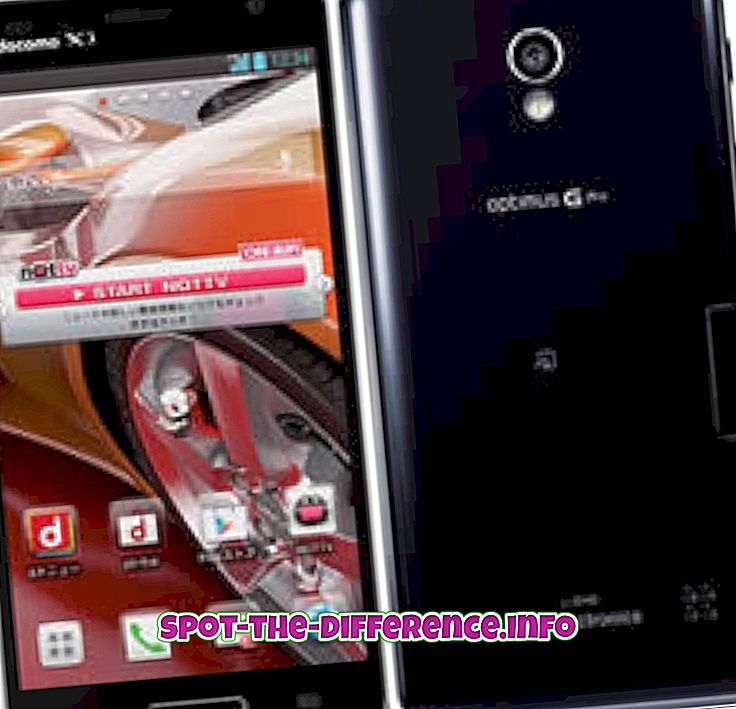
Hovedforskjell: Diffusjon er prosessen som molekyler beveger seg og reiser fra ett sted til et annet uten å kreve bulkbevegelse. Effusjon er prosessen som molekyler beveger seg gjennom et pinhull fra et sted med høy konsentrasjon til lav konsentrasjon.
Vilkårene diffusjon og effusjon er ofte brukt i mange vitenskaper som kjemi, fysikk og biologi. I kjemi er disse to begrepene to egenskaper av gasser. Disse to er forvirrende for mange mennesker som bare lærer det grunnleggende av gasser og dets egenskaper. Diffusjon og Effusjon er to forskjellige termer som betyr to forskjellige ting og bør ikke brukes om hverandre. Diffusjon refererer til gassens evne til å blande seg med hverandre, mens effusjon refererer til gassens evne til å bevege seg gjennom et lite pinhull. Diffusjon er også brukt i sosiologi, økonomi og finans for å referere til diffusjon av mennesker, ideer og verdier.
Diffusjon er prosessen der molekyler beveger seg og reiser fra ett sted til et annet uten å kreve bulkbevegelse. Diffusjon resulterer i at molekyler beveger seg eller blander ved kun å bruke kinetisk energi. Ordet "diffusjon" er hentet fra det latinske ordet "diffundere" som betyr "å spre seg". I diffusjon er molekyler i konstant bevegelsesstatus, og når de drives av kinetisk eller termisk energi, pleier de å blande seg med andre molekyler som resulterer i en uadskillelig blanding. La oss ta en praktisk tilnærming, en beholder er delt i A & B seksjoner ved hjelp av en solid partisjon; Den første delen er fylt med vann, mens den andre delen er fylt med rødt fargestoff. Nå, når partisjonen løftes, prøver fargen og vannet å fylle hele beholderen. Derefter farger fargen langsomt vannet rødt, dette er diffusjon.
Diffusjon fører til at molekylene skifter fra et høyere konsentrasjonsareal til et lavere konsentrasjonsareal, noe som resulterer i blandingen av alle molekylene. Diffusjon stopper når alle molekylene er jevnt fordelt. Diffusjon er ikke begrenset til vann og fungerer best i gassformige tilstander, der molekyler har mer energi og evne til å blande seg med andre molekyler. Det er to tilnærminger til diffusjon: fenomenologisk og atomistisk. Ifølge fenomenologisk tilnærming reiser molekylene fra regioner med høyere konsentrasjon til regioner med lavere konsentrasjon. I den atomistiske tilnærmingen anses diffusjon som følge av tilfeldig spasertur av de diffuserende partiklene, hvor diffusjonen drives av termisk energi som får dem til å blande seg sammen. Diffusjon spiller en viktig rolle i å skape mineraler, næringsstoffer og energi som kreves av kroppen.

Effusjon er prosessen som molekyler beveger seg gjennom et pinhull fra et sted med høy konsentrasjon til lav konsentrasjon. Prosessen beskriver gassens evne til å bevege seg gjennom et lite hull uten kollisjoner mellom molekyler. Dette skjer når diameteren av hullet er betydelig mindre enn molekylets gjennomsnittlige frivei. Den gjennomsnittlige friveien er den gjennomsnittlige avstanden som er reist av en bevegelig partikkel mellom suksessive kollisjoner. Et praktisk eksempel på dette ville være å fylle en beholder med en flaske med røyk og kaste et lite hull i flasken, røyken som begynner å pore ut av hullet betraktes som effusjon.
Ifølge den skotske kjemikeren Thomas Graham, som opprettet formelen for måling av effusjon, har det skapt en Graham-lov som bestemmer hvor fort gassen vil reise og hvordan den kan måles. I henhold til Grahams lov, er hastigheten ved hvilken utslipp av gasser er avhengig av deres molekylvekt. Gassen med en lavere molekylvekt vil utløse raskere enn en gass med høyere molekylvekt. Effusjon beregnes ved å måle hvor mange molekyler som går gjennom hullet på et sekund. På samme måte, i termodynamikken, er effusjonshastigheten av en gass omvendt proporsjonal med kvadratroten av massen av partiklene.