Hovedforskjell: Molaritet, også kjent som molar konsentrasjon, måler antall mol av et stoff som er tilstede i per liter løsning. Molarity er betegnet med en hovedstad M. Molality måler antall mol av et stoff som er tilstede i per kilo løsemiddel. Molality er betegnet med små bokstaver m.
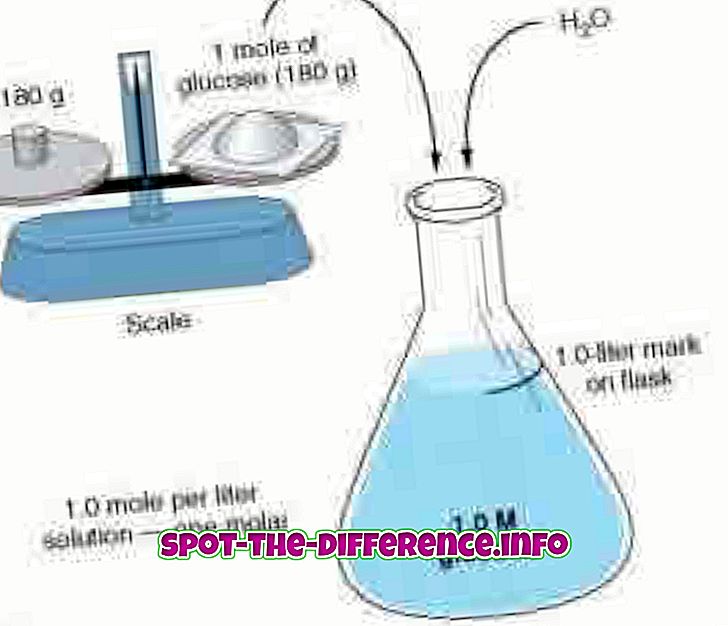
Begge konseptene baserer sine beregninger på hvor mange mol er tilstede i den nåværende løsningen. En løsning kan defineres som en homogen blanding, noe som betyr at to eller flere komponenter er blandet til det punktet at det ikke kan skilles fra det blotte øye. Disse to konseptene krever forståelse av mol som det bestemmer antall mol tilstede i løsningen. Teorien om mol ble oppdaget av italiensk forsker Amedeo Avogardo.
I 1811 foreslo Avogardo at volumet av gass, ved en gitt temperatur og trykk, er proporsjonal med antall atomer eller molekyler uavhengig av dens natur. Dette konseptet er kjent som Avogardo-konstanten. Det er definert som antall bestanddeler (vanligvis atomer eller molekyler) i en mol av en gitt substans. I legemet vil en mol av et stoff representere antall atomer og molekyler tilstede i elementet. For eksempel: Oksygen har en atomvekt på 16, dette vil representere mengden per mol oksygen. Så ville en mol oksygen ha en masse på 16 gram. Ifølge Avogardo ville en mol oksygen ha det samme antall atomer som en mol hydrogen. Imidlertid kan de variere i vekt.
Molaritet og molalitet måler konsentrasjonen ved hjelp av to forskjellige tilnærminger. Molaritet, også kjent som molar konsentrasjon, måler antall mol av et stoff som er tilstede i per liter oppløsning. Molaritet er betegnet med en hovedstad M. Så en løsning med 1, 0 M vil angi at den inneholder 1 mol løsemiddel per liter løsning. For eksempel: En løsning av vann og sukker. Hvis løsningen måles som 1, 0 M, har løsningen 1 mol sukker pr. Liter oppløsning tilstede. Molaritet er også kjent som konsentrasjon av innholdsstoffer, mengde konsentrasjon, stoffkonsentrasjon eller bare konsentrasjon. Molariteten kan beregnes ved å bruke formelen: M = mol (# mol) / L (volum av oppløsning i liter).

Molality måler antall mol av et stoff som er tilstede i kilo løsemiddel. Molality er betegnet med små bokstaver m. Så en løsning med 1, 0m vil angi at den inneholder 1 mol løsemiddel per kilo løsemiddel. La oss skille opp løsningen fra løsemiddel. Solute er stoffet som blir oppløst i et annet stoff. Et løsemiddel er et stoff som løser oppløsningen. Så, hvis vann og sukker blandes sammen, ville sukker være løsemiddel og vann løsningsmidlet. Det blandede sukkervannet ville være løsningen. Nå, i molalitet, er det av største betydning at molene er delt av løsningsmiddelets masse og ikke løsningen. Molalitet kan beregnes ved hjelp av formelen: m = mol (# mol) / KG (masse løsningsmiddel i kg).
Hvorfor forskjellen? Vel, begge brukes når de håndterer temperatur. Hvis en løsning kommer til å endres i temperatur, brukes molalitet. Men for løsninger som forblir ved konstant temperatur brukes molaritet. Dette skyldes at når temperaturen stiger eller faller, endres volumet av løsningen og dette påvirker direkte molariteten. Derfor brukes molalitet til å beregne konsentrasjon.